Test autodiagnostico rapido per la rilevazione qualitativa degli antigeni della proteina Nucleocapside di SARS-CoV-2 in campioni nasali umani.
Inserito nella lista dei tamponi rapidi per autotest della regione Emilia Romagna.

Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) è stato riconosciuto come il virus responsabile della pandemia di COVID-19.
approfondisciCome per altre malattie respiratorie, il virus SARS-CoV-2 può causare un’infezione asintomatica, sintomi moderati come, ad esempio, raffreddore, mal di gola, tosse e febbre, perdita del gusto e/o dell’olfatto, fino a sintomi più gravi come polmonite e difficoltà respiratorie con risvolti anche letali. Il periodo d’incubazione di SARS-CoV-2 può variare da 1 a 14 giorni.
COVID-19 ANTIGEN SELF-TEST è indicato per chiunque voglia verificare un’eventuale infezione da SARS-CoV-2 in corso.
approfondisciI test antigenici per COVID-19 permettono di effettuare una rilevazione qualitativa di SARS-CoV-2 in campione nasali e si configurano come dispositivi diagnostici rapidi da effettuare ad uso domestico. Si consiglia di utilizzare COVID-19 ANTIGEN SELF-TEST durante l’arco temporale relativo alla possibile esposizione al virus.
COVID-19 ANTIGEN SELF-TEST è un dispositivo immunocromatografico per la rilevazione qualitativa di antigeni Nucleocapside in campioni nasali.
| Specificità | 99,3% |
| Sensibilità | 93,5% |
| Accuratezza | 97,6% Specificità soggetti sintomatici |
| Specificità soggetti asintomatici | 99% |
| Sensibilità soggetti sintomatici | 97,2% |
| Sensibilità soggetti asintomatici | 97,8% |
| Accuratezza soggetti sintomatici | 98,6% |
| Accuratezza soggetti asintomatici | 98,4% |



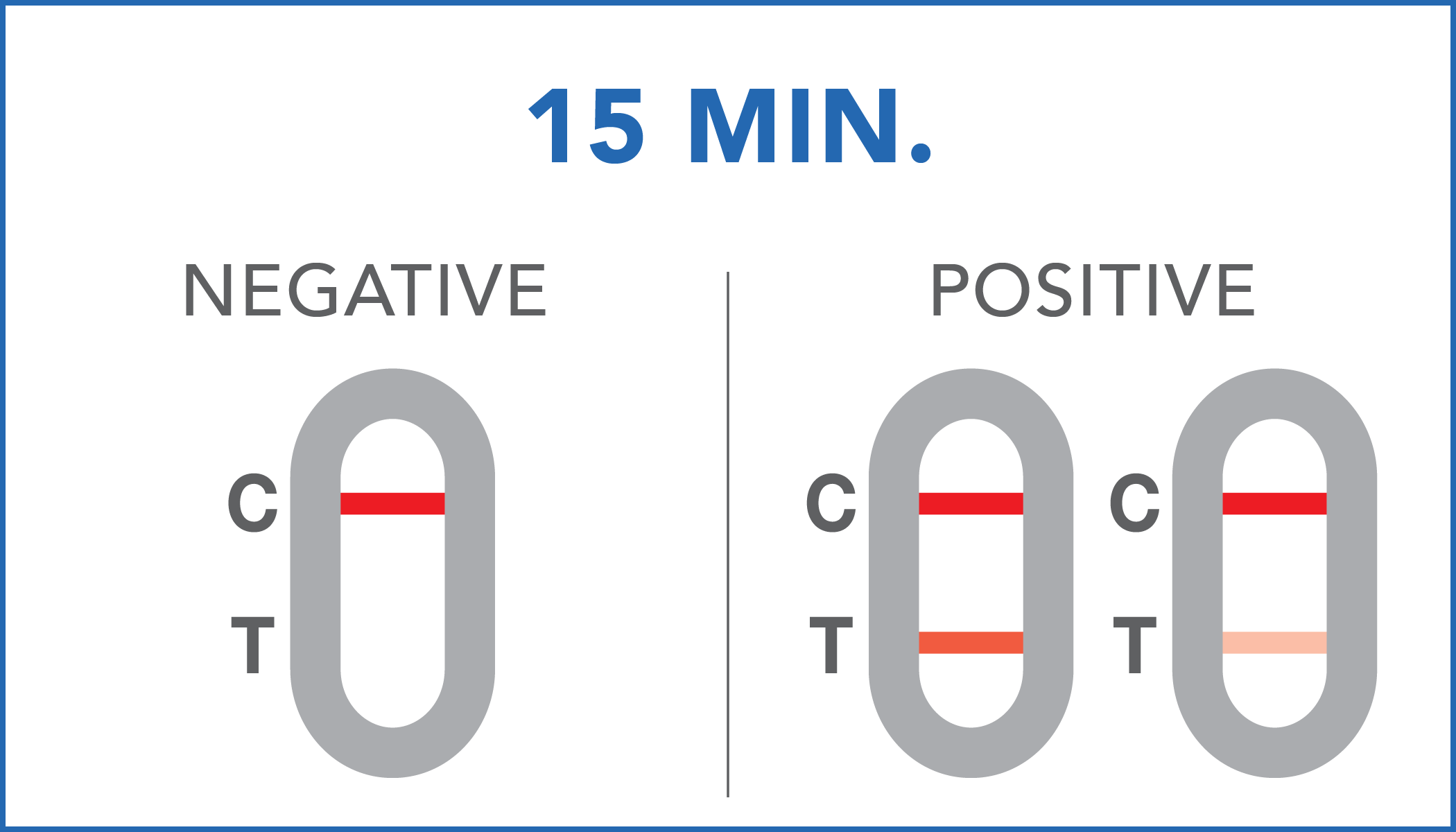
| Negativo | i livelli di antigeni SARS-CoV-2 non sono presenti nel campione oppure lo sono in concentrazioni molto basse, non rilevabili dal dispositivo. |
| Positivo | gli antigeni SARS-CoV-2 sono stati rilevati dal sistema diagnostico. È suggerito contattare uno specialista o il dipartimento sanitario locale per approfondimenti. |
1. Diagnosis and Treatment Protocol for Novel Coronavirus Pneumonia (Trial Version 7). National Health Commission & National Administration of Traditional Chinese Medicine 2020.
2. WHO Director-General’s opening remarks at the media briefing on COVID-19 - 11 March 2020 (https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---11-march-2020)
3. Centers for Disease Control and Prevention, Interim Guidelines for Collecting, Handling, and Testing Clinical Specimens for COVID-19 (https://www.cdc.gov/coronavirus/2019-ncov/lab/guidelines-clinicalspecimens.html)
4. European Centre for Disease Prevention and Control. Options for the use of rapid antigen tests for COVID-19 in the EU/EEA - first update. 2021. https://www.ecdc.europa.eu/en/publications-data/optionsuse-rapid-antigentests-covid-19-eueea-first-update
5. WHO, Advice on the use of point-of-care immunodiagnostic tests for COVID-19
https://www.who.int/ news-room/commentaries/detail/advice-on-the-use-ofpoint-of-care-immunodiagnostic-tests-for-covid-19
6. Council of the European Union, Council Recommendation on a common framework for the use and validation of rapid antigen tests and the mutual recognition of COVID-19 test results in the E, 20 January 2021
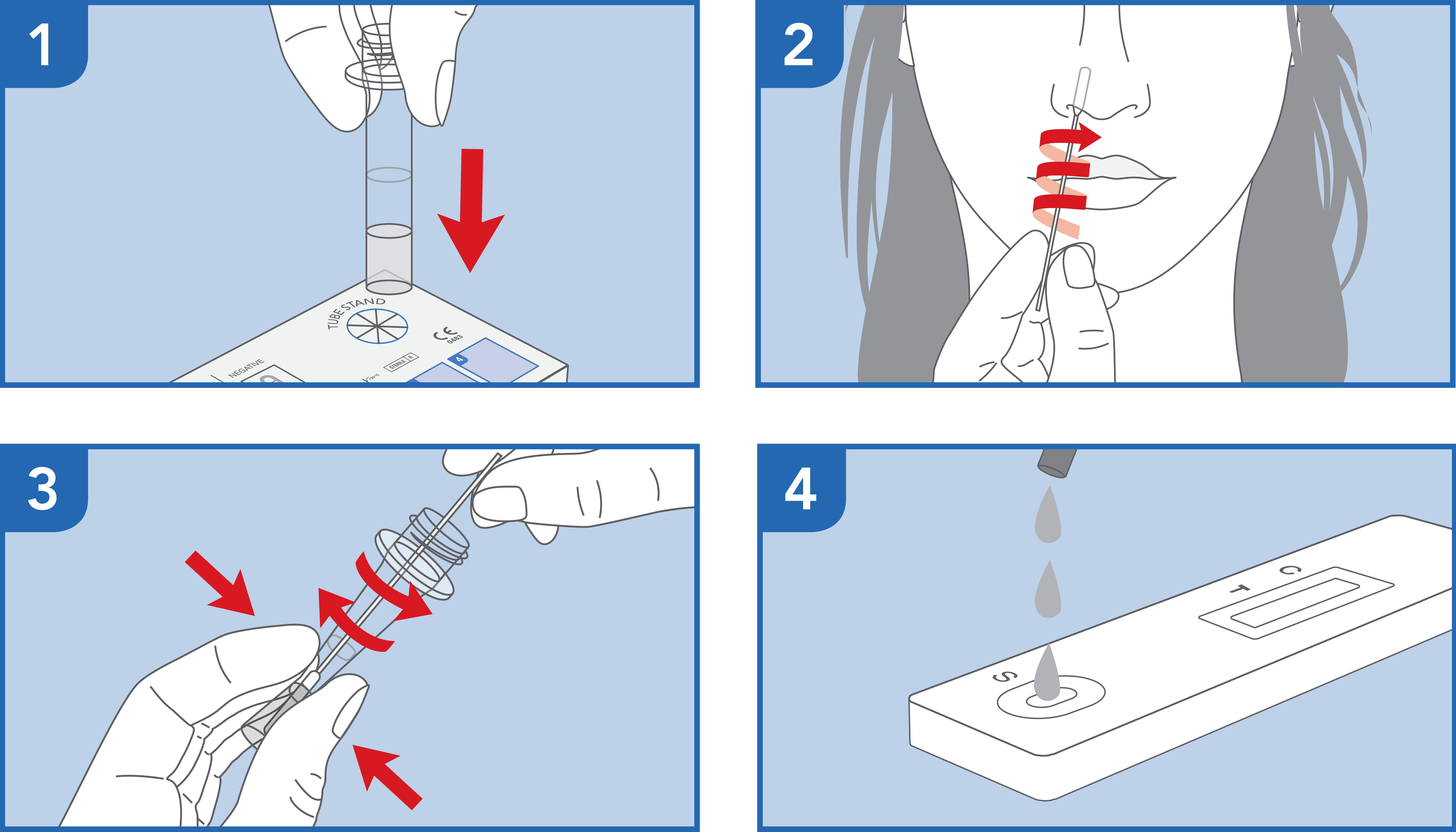
Il test è stato effettuato correttamente nel momento in cui vengono seguite le istruzioni per l'uso, compreso il tempo di lettura e interpretazione dei risultati indicato in procedura, alla sezione "INTERPRETAZIONE DEI RISULTATI" delle istruzioni per l'uso.
Si consiglia di eseguire il test in presenza di sintomi riconducibili a COVID-19, oppure qualora si sospetti di essere venuti a contatto con soggetti positivi negli ultimi 5 giorni.
L'intensità di colore delle bande di controllo e di test può variare a seconda della concentrazione di antigeni presenti nel campione. Pertanto, qualsiasi tonalità di colore nella regione di test (T) deve essere considerata positiva.
Verificare la disponibilità del prodotto con il rappresentante locale nel proprio paese